Введение
Бременем современного урогинекологического сообщества является вопрос использования синтетических материалов в хирургии тазового дна. Непрекращающиеся дискуссии и споры о целесообразности применения имплантов в условиях генитального пролапса, недержания мочи до сих пор не привели к формированию универсального алгоритма или тактики ведения пациентов с дисфункцией тазового дна.1 С одной стороны, коррекция пролапса тазовых органов за счет сетчатых протезов сопряжена с риском возникновения mesh-ассоциированных (связанных с имплантацией протеза – mesh) осложнений, с другой – пластика стенок влагалища собственными тканями имеет больший процент возникновения рецидивных форм.2,3
Несмотря на определенные недоговоренности среди различных международных и отечественных медицинских сообществ, хирургическое лечение стрессового недержания мочи с помощью установки уретральных слингов в большинстве случаев признается в качестве наиболее эффективного и безопасного метода коррекции.4,5 Казалось бы, оптимальный доступ и оперативная техника в данном сегменте урогинекологии найдены, однако в последнее время накапливаются данные многоцентровых исследований, свидетельствующих о возникновении признаков хронической тазовой боли, преимущественно в виде диспареунии и сексуальной дисфункции, манифестирующих в отдаленном послеоперационном периоде вне зависимости от позадилонного или трансобтураторного доступа.6,7
Возвращаясь к проблеме mesh-ассоциированных осложнений следует отметить, что данное понятие включает симптомокомплекс, значительно снижающий качество жизни и способствующий социальной дезадаптации, психоэмоциональной дестабилизации, помимо ярко выраженной или латентной клинической симптоматики.8,9 К таким осложнениям, как правило, относят экспозицию импланта при его визуальном определении, сморщивание импланта, хроническую тазовую боль.10 Безусловно, возникновение таких неблагоприятных проявлений не только снижает удовлетворенность качеством оказанной медицинской помощи, но и требует дополнительного воздействия, нередко при помощи повторного оперативного вмешательства с иссечением сетчатого импланта и решением вопроса о дальнейшей тактике ведения в послеоперационном периоде.
Также актуальным является и проблема развития mesh-осложнений инфекционного генеза, что, как правило, проявляется в виде патологических выделений из половых путей, локальной болезненностью, уплотнением, припухлостью и отеком, покраснением и различными общеклиническими симптомами.11 Частота возникновения таких осложнений в литературе варьирует от 1% до 68% в зависимости от вида хирургического вмешательства, типа синтетического материала, выраженности ответной реакции организма и наличия сопутствующей коморбидной патологии.12
Попытки изучить взаимосвязь влагалищной микробиоты и риска развития инфекционно-воспалительных заболеваний после имплантации сетчатых протезов привели к выводам о том, что исходно основную часть микробиома составляют Лактобактерии, конкурентно ингибирующие рост остальных условно-патогенных микроорганизмов.13 При сравнении изменений микробиома среди пациентов, у которых развились mesh-ассоциированные осложнения, преимущественно в виде экструзии и сморщивания импланта, и пациентов с неосложненным течение послеоперационного периода было выявлено, что рост колоний Вейлонеллы и Актиномицет является фактором риска неблагоприятных исходов хирургического лечения.14 При этом авторы исследования отмечают, что достоверных признаков ассоциации влагалищного дисбиоза и mesh-осложнений выявлено не было, однако нельзя не отметить тесную взаимосвязь диссоциации нормальной микробиоты влагалища у пациентов с развитием экструзии или сморщивания сетчатого протеза.
Таким образом, хирургия генитального пролапса и недержания мочи находится в постоянном движении и совершенствовании, вследствие чего изучение факторов риска и механизмов развития mesh-ассоциированных осложнений позволит улучшить и модернизировать имеющиеся алгоритмы ведения. При этом важным элементом рационального лечения пациентов с пролапсом тазовых органов является не только обеспечение оптимального хирургического воздействия, но и грамотное выстраивание послеоперационного периода с целью наиболее благоприятного восстановления тканей и улучшения репаративных свойств.
Цель исследования
Целью исследования явилось улучшение исходов комбинированной коррекции генитального пролапса и стрессового недержания мочи с использованием собственных тканей и имплантацией уретрального слинга за счет минимизации риска mesh-ассоциированных осложнений путем назначения в послеоперационном периоде спрея Эпиген Интим в качестве иммуностимулирующего, противовоспалительного и регенерирующего средства.
Материалы и методы исследования
Исследование включило 60 пациенток перименопаузального периода с признаками генитального пролапса 2 и более стадии по классификации POP-Q по переднему и заднему компартментам тазового дна и недержания мочи стрессового характера.
С целью верификации мочевой инконтиненции стрессового характера и исключения альтернативных вариантов недержания мочи нами выполнялось: сбор анамнеза и жалоб, проба Вальсальвы во время выполнения гинекологического осмотра, консультация врача-уролога.
Критерии включения: цистоцеле и/или ректоцеле 2 и более стадии по POP-Q, стрессовое недержание мочи.
Критерии исключения: мультикомпартментное поражение тазового дна (с поражением апикального отдела); предшествующая хирургическая коррекция пролапса или недержания мочи с использованием синтетических материалов; смешанные формы недержания мочи.
Всем пациентам проводилось стандартное обследование в рамках предоперационной подготовки: сбор анамнестических данных, клинический анализ крови, биохимический анализ крови, коагулограмма, электрокардиографическое исследование, консультация терапевта, гинекологический осмотр, двуручное влагалищно-абдоминальное обследование, ультразвуковое исследование органов малого таза и молочных желез. Статистически значимых различий между группами выявлено не было.
Госпитализация пациентов осуществлялась за день до предполагаемого вмешательства. В условиях стационара производилась стратификация риска тромбоэмболических осложнений и соответствующая профилактика в объеме механической компрессии вен нижних конечностей и подкожного введения профилактических доз низкомолекулярного гепарина в зависимости от индекса массы тела. Накануне вечером пациентам проводилась механическая подготовка кишечника с помощью очистительной клизмы. На основании имеющихся алгоритмов антибиотикопрофилактики за 1 час до начала операции производилось внутривенное введение препаратов широкого спектра, преимущественно цефалоспоринового ряда, при наличии аллергической реакции в анамнезе назначался амоксициллина клавулонат или ципрофлоксацин.15,16,17
Коррекция цисто- или ректоцеле осуществлялась по стандартной технике влагалищным доступом с использованием собственных тканей и техники субфасциальной диссекции, в качестве шовного материала использовались рассасывающиеся нити полипропиленовой конструкции. Ушивание краев слизистой производилось с помощью наложения узловых швов, а задняя кольпоррафия дополнялась выполнением перинеоррафии с целью восстановления нормальной анатомической структуры тазового дна.
Коррекция недержания мочи производилась с использованием сетчатого импланта в виде уретрального слинга по классической технике трансобтураторного доступа. С целью последующего контроля натяжения сетчатого импланта нити укрывались при помощи антисептической повязки. На 1 сутки послеоперационного периода производился контроль натяжения, при отсутствии или минимальном количестве остаточной мочи по данным ультразвукового исследования производилось удаление мочевого катетера и иссечение контрольных нитей слинга. При необходимости выполнялось ослабление или натяжение импланта за счет расслабления или подтягивания контрольных нитей, после чего также производилось их иссечение.
Тактика послеоперационного периода основывалась на обеспечении ранней активизации и ускоренного восстановления. Распределение пациентов производилось методом простой рандомизации в зависимости от тактики послеоперационного ведения (рис. 1).
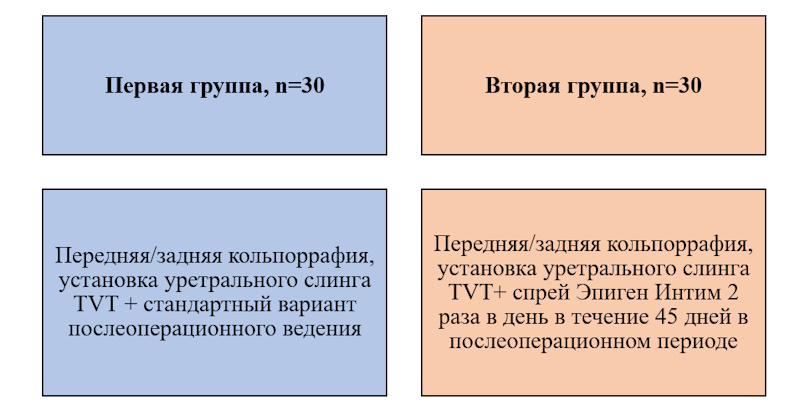
Рисунок 1. Дизайн исследования (n=60)
Стандартный вариант послеоперационного ведения включал обработку наружных половых органов и послеоперационных швов с помощью водного раствора хлоргексидина биглюконата 2 р/сутки в течение 10 дней, половой и физический покой 30 дней, наблюдение гинеколога по месту жительства. В модифицированной схеме среди пациентов второй группы использовался спрей Эпиген Интим в пролонгированном режиме - 2 р/сутки в течение 45 дней. Спрей Эпиген Интим был выбран нами, учитывая наличие в его составе активированной глицирризиновой кислоты, обладающей иммуностимулирующим, регенерирующим и противовоспалительным свойствами за счет стимуляции выработки интерферонов, повышения активности Т-клеточного звена иммунитета, ингибирующего воздействия на выработку кининов и простагландинов в зоне воспаления.18,19
Таблица 1. Основные показатели среди пациенток обеих групп, n=60
| Параметры | Первая группа n=30 | Вторая группа n=30 | p |
| Возраст (среднее значение + среднеквадратичное отклонение) | 48.20 (±4.88) | 47.62 (±6.24) | >0,2 |
| Индекс массы тела (среднее значение + среднеквадратичное отклонение) | 24.80 (±2.56) | 25.90 (±5.21) | >0,3 |
| Койко-день, среднее значение | 3.8 | 3.3 | >0,1 |
Пациенты обеих групп статистически не различались по возрасту и индексу массы тела, а среднее значение продолжительности госпитализации составило не более 4 койко-дней, при этом во второй группе отмечалось незначительное уменьшение длительности госпитализации (в первой группе среднее значение 3.8, во второй – 3.3) [табл. 1].
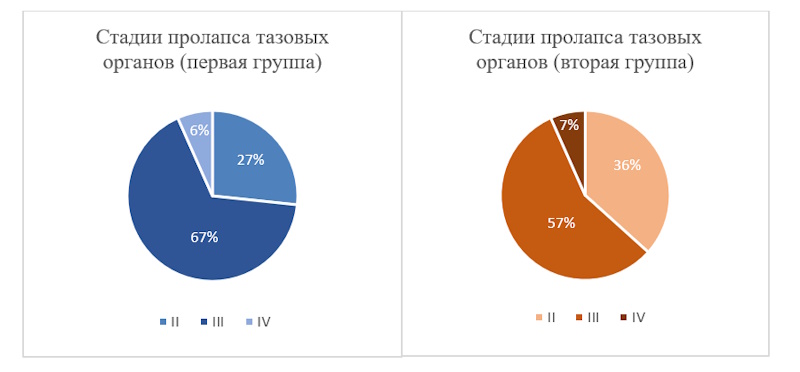
Рисунок 2. Стадирование генитального пролапса на основании классификации POP-Q, n=60
На основании классификации Pelvic Organ Prolapse Quantification System (POP-Q) в структуре генитального пролапса у 20 пациенток (67%) первой группы и 17 пациенток (57%) второй группы определялись признаки опушения передней и/или задней стенок влагалища 2 стадии (рис. 2). Генитальный пролапс 3 стадии обнаруживался в 27% случаев в первой группе и в 36% во второй группе.
Основными жалобами среди пациенток обеих групп явились: ощущение инородного тела во влагалище или промежности (72% в первой группе, 71% во второй группе), хроническая тазовая боль в виде диспареунии (17% и 21% соответственно), а также констипация и/или дизурические явления обструктивного типа (11% и 9% соответственно) [рис. 3]. При этом также все пациентки обеих групп предъявляли жалобы на недержание мочи при кашле, чихании, выполнении физических нагрузок.
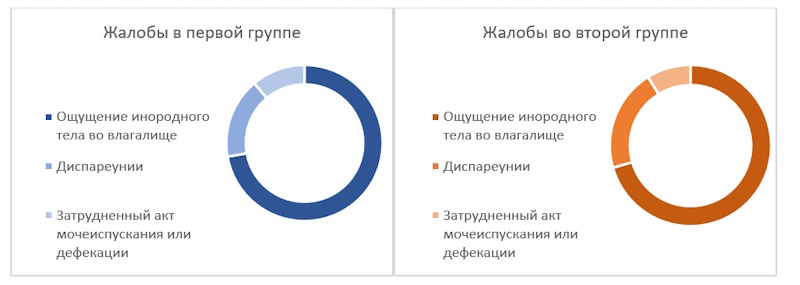
Рисунок 3. Характеристика жалоб среди пациенток обеих групп, n=60
С целью обнаружения взаимосвязи между изменениями микробиома влагалища и риском возникновения mesh-ассоциированных осложнений нами был проведен сравнительный анализ исходов послеоперационного периода на основании динамики клинических проявлений генитального пролапса, недержания мочи и соответственно эффективности проводимого хирургического лечения; вероятности развития mesh-осложнений; данных микроскопического исследования влагалищного отделяемого и биоценоза влагалища методом ПЦР у пациентов как с осложненным, так и неосложненным течением послеоперационного периода.
Статистическая обработка полученных результатов осуществлялась с применением пакета прикладных программ STATISTICA 10 (StatSoft, 2012), Office Excel (Microsoft, 2019). Статистически достоверным считались изменения показателей с вероятностью ошибки менее 0,05.
Результаты
На основании проведенного хирургического лечения в объеме передней и/или задней кольпоррафии и установки уретрального слинга производилась оценка динамики жалоб и риска mesh-ассоциированных, инфекционных осложнений на момент выписки из стационара и через 45 дней после проведенного лечения (рис. 4, 5).
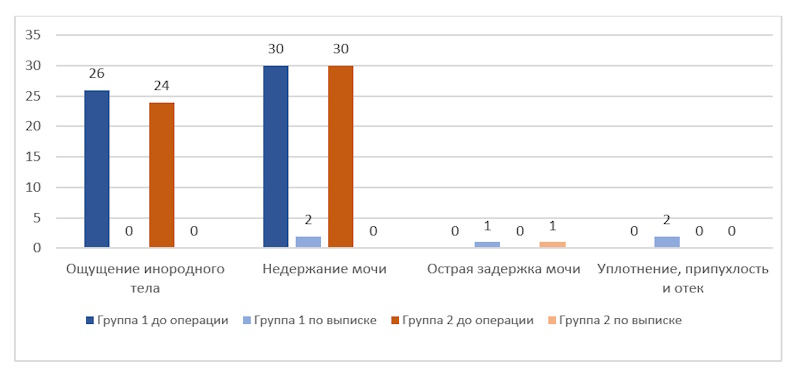
Рисунок 4. Динамика жалоб и клинических проявлений среди пациенток обеих групп на момент выписки из стационара, n=60
Согласно анализу клинических проявлений по выписке из стационара следует отметить, что в 2 случаях (6,7%) среди пациентов первой группы отмечались признаки недержания мочи смешанного характера (p<0,05 между первой и второй группами: 6,7% и 0 соответственно), при этом следует отметить, что указанные симптомы имели легкий характер выраженности и не повлияли на удовлетворенность пациентами качеством жизни, но были направлены под наблюдение уролога в послеоперационном периоде. Также в единичных случаях как в первой, так и во второй группе отмечались признаки острой задержки мочи на 1-2 сутки послеоперационного периода, что потребовало ослабления нитей слинга и стимуляции диуреза с полностью обратимым течением. В 6,7% случаев (n=2) среди пациенток первой группы (p<0,05 между первой и второй группами: 6,7% и 0 соответственно) выявлялись признаки инфекционных mesh-ассоциированных осложнений в виде уплотнения и припухлости в области имплантации слинга, что также сопровождалось патологическими выделениями из половых путей. При этом пациентам была назначена антибактериальная терапия цефалоспоринами в пролонгированном режиме на 5 дней до момента купирования указанных жалоб.
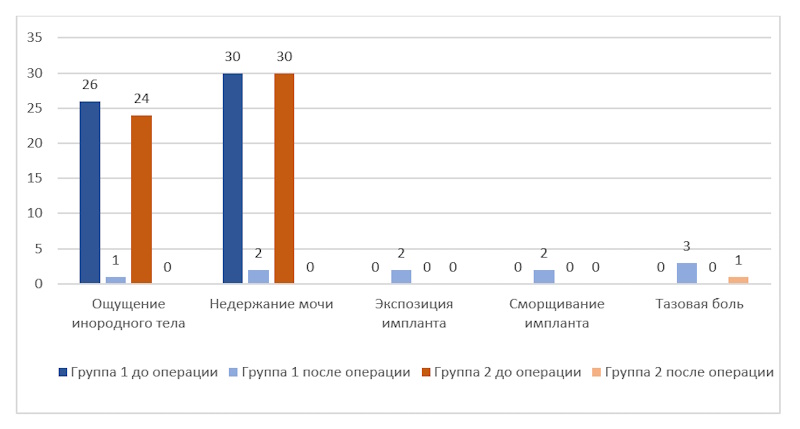
Рисунок 5. Динамика жалоб и клинических проявлений среди пациенток обеих групп через 45 дней послеоперационного периода, n=60
В результате оценки жалоб и клинической симптоматики через 45 после проведенного хирургического лечения отмечалось, что у 3 пациенток (10%) первой группы отмечались признаки mesh-ассоциированных осложнений в виде экспозиции и сморщивания импланта (2 пациента – 6,7%; p<0,05 между первой и второй группами: 6,7% и 0 соответственно), что потребовало иссечения сетчатого протеза в дальнейшем. Также среди пациентов первой группы в 3 случаях имелись жалобы на тазовую боль, при этом во второй группе лишь в 1 случае (3,3%).
Таблица 2. Показатели микроскопического исследования влагалищного отделяемого через 45 дней после проведенного лечения, n=60
| Параметры (V) | Группа 1, неосложненное течение, n=27 | Группа 1, осложненное течение, n=3 | Группа 2, n=30 |
| Эпителий | Умеренное кол-во | Скудное кол-во | Умеренное кол-во |
| Лейкоциты, п/зр | 20-30 | 70-80 | 10-20 |
|
p<0,05 |
|||
| Слизь | Умеренное кол-во | В большом количестве | Умеренное кол-во |
| Флора (вид) | Полиморфная палочка | Смешанная | Полиморфная палочка |
| Флора (количество) | Умеренное кол-во | Умеренное кол-во | Умеренное кол-во |
При проведении микроскопического исследования среди пациенток обеих групп было выявлено, что наличие mesh-ассоциированных осложнений сопряжено с увеличением как количества лейкоцитов, так и соотношения лейкоцитов к эпителиальным клеткам при сравнении с неосложненным течением послеоперационного периода в первой группе и пациентами из второй группы (табл. 2).
Таблица 3. Показатели исследования биоценоза влагалища методом ПЦР через 45 дней после проведенного лечения, n=60
| Параметры, средние значения | Группа 1, неосложненное течение, n=27 | Группа 1, осложненное течение, n=3 | Группа 2, n=30 |
| Общая бактериальная масса | 106,2 | 106,0 | 106,3 |
|
Нормофлора |
|||
| Lactobacillus spp. | 68,61% | 37,8% | 78,32% |
| p<0,05 p<0,05 | |||
| Факультативно-анаэробные микроорганизмы | |||
| Enterobacterium spp. | 0,18% | 2,37% | 0,51% |
| p<0,05 p 0,045 | |||
| Staphylococcus spp. | 1,8% | 6,2% | 2,3% |
| p<0,05 | p<0,05 | ||
| Облигатно-анаэробные микроорганизмы | |||
| Gardnerella vaginalis + Prevotella bivia + Porphyromonas spp. | 1,3% | 8,83% | 0,65% |
| p<0,01 p<0,01 | |||
| Eubacterium spp. | 1,1% | 1,4% | 0,89% |
| Sneathia spp. + Leptotrichia spp. + Fusobacterium spp. | 1,58% | 3,64% | 1,7% |
| Megasphaera spp. + Veillonella spp. + Dialister spp. | <0,1% | 9,72% | <0,1% |
| p<0,01 p<0,01 | |||
| Atopobium vaginae | <0,1% | <0,1% | <0,1% |
При исследовании данных биоценоза влагалища методом полимеразно-цепной реакции через 45 дней после проведенного лечения было выявлено, что среди пациенток с осложненными формами из 1 группы (n=3, пациентки с экспозицией и сморщиванием импланта) имелись признаки неспецифического вульвовагинита, проявляющегося снижением количества нормофлоры в виде лактобактерий, повышением концентрации как факультативно-анаэробных, так и облигатно-анаэробных микроорганизмов (табл. 3).
При сравнительном анализе результатов ПЦР исследования среди пациенток обеих групп отмечается, что соотношение нормофлоры к остальным условно-патогенным микроорганизмам более благоприятное у пациенток второй группы, которым производилась пролонгированная обработка послеоперационной зоны с помощью спрея Эпиген Интим в течение 45 дней [содержание Lactobacillus spp. в первой группе с неосложненным течением 68,61%, во второй группе 78,32% (p<0,05)], при этом при осложненном течении послеоперационного периода наблюдается достоверное угнетение нормофлоры по сравнению с пациентами как первой, так и второй группы (37,8% против 68,61% и 78,32% соответственно).
Также нельзя не отметить повышение концентрации облигатно-анаэробной флоры под представительством Veillonella spp. и Gardnerella vaginalis в условиях осложненного течения реабилитационного периода (9,72% против концентрации <0,1% среди неосложненных пациентов; 8,83% против 1,3% в первой группе и 0,65% во второй группе).
Обсуждение результатов
Хирургическое лечение генитального пролапса и недержания мочи сопряжены с рядом рисков и осложнений, ассоциированных не только со сложностью техники корригирующего вмешательства, но и с имплантацией сетчатого импланта.2,3 Различные методики влагалищной хирургии тазового дна не раз подвергались критике на основании повышенной вероятности возникновения неблагоприятных послеоперационных исходов при использовании синтетических материалов, что привело мировое сообщество к заключению о большей безопасности применения mesh-less (без сетчатых протезов) техник или коррекции собственными тканям.1,4 Установка уретральных слингов при стрессовом недержании мочи наряду с лапароскопическими вариантами хирургии не сопряжены с повышенным риском осложнений, что предпочтительно при рассмотрении варианта лечения генитального пролапса и мочевой инконтиненции с использованием имплантов.5,6
Несмотря на непрекращающееся развитие оперативных техник, улучшение особенностей и структуры сетчатых материалов, риск развития mesh-ассоциированных осложнений продолжается оставаться беременем современной урогинекологии.8-10 Работы Fettweis J.M. (2012), Veit-Rubin N. (2019) и соавторов продемонстрировали влияние не только композитного состава импланта, но и влагалищного микробиома на вероятность возникновения осложнений, связанных с имплантацией, что требует более персонализированного подхода перед планированием оперативного вмешательства в зависимости от предрасположенности и коморбидности пациента.13,14
В нашем исследовании мы провели сравнительный анализ результатов хирургического лечения опущения передней/задней стенок влагалища в сочетании со стрессовым недержанием мочи при помощи традиционного и модифицированного способа периоперационного ведения. Модификация тактики заключалась в пролонгированном воздействии антисептического, противовоспалительного спрея Эпиген Интим в течение 45 дней послеоперационного периода среди пациенток второй группы с целью улучшения репаративных свойств тканей и благоприятного воздействия на микробиом влагалища.
При анализе динамики клинических проявлений на момент выписки из стационара было отмечено, что в 2 случаях (6,7%) среди пациентов первой группы отмечались признаки недержания мочи смешанного характера (p<0,05 между первой и второй группами: 6,7% и 0 соответственно), а в 6,7% случаев (n=2) среди пациенток первой группы (p<0,05 между первой и второй группами: 6,7% и 0 соответственно) выявлялись признаки инфекционных mesh-ассоциированных осложнений в виде уплотнения и припухлости в области имплантации слинга, что также сопровождалось патологическими выделениями из половых путей и потребовало назначения антибактериальной терапии. Контрольный осмотр через 45 дней выявил, что у 3 пациенток (10%) первой группы отмечались признаки mesh-ассоциированных осложнений в виде экспозиции и сморщивания импланта (2 пациента – 6,7%; p<0,05 между первой и второй группами: 6,7% и 0 соответственно), что потребовало иссечения сетчатого протеза в дальнейшем.
В результате проведенного микроскопического исследования влагалища в рамках контрольного осмотра было обнаружено, что наличие mesh-ассоциированных осложнений сопряжено с увеличением как количества лейкоцитов, так и соотношения лейкоцитов к эпителиальным клеткам (Лейкоциты (п/зр) 70-80 против 20-30 и 10-20 в первой и второй группах, p<0,05). А анализ влагалищного микробиома методом ПЦР продемонстрировал угнетение представителей нормофлоры на фоне роста условно-патогенных микроорганизмов среди пациентов с экспозицией и сморщиванием импланта (37,8% лактобактерий против 68,61% и 78,32% в первой и второй группах; 9,72% Veillonella spp. против концентрации <0,1% среди неосложненных пациентов; 8,83% Gardnerella vaginalis против 1,3% в первой группе и 0,65% во второй группе).
Таким образом, отмечается определенная взаимосвязь между состоянием влагалищного микробиома и репарацией тканей после имплантации синтетических материалов, что находится в прямой ассоциации с риском развития осложнений, связанных с использованием имплантов. При этом содержание Lactobacillus spp. в первой группе с неосложненным течением составило 68,61%, во второй группе 78,32% (p<0,05), что также свидетельствует о более благоприятном воздействии модифицированной схемы послеоперационной тактики с использованием спрея Эпиген Интим в пролонгированном режиме.
Заключение
Хирургическая коррекция генитального пролапса и недержания мочи с применением синтетических имплантов требует рационализированного подхода, что определяет не только обеспечение оптимального доступа и метода оперативного вмешательства, но и грамотно выстроенную послеоперационную тактику.
Использование специализированных препаратов, например спрея Эпиген Интим с противовоспалительным, иммуностимулирующим и регенерирующим действием, в пролонгированном режиме после операции позволяет адаптировать состояние влагалищного микробиома, что сопряжено со снижением риска mesh-ассоциированных осложнений.
Дальнейшие исследования по анализу микрофлоры влагалища перед операцией и в послеоперационном периоде могут позволить дифференцировать профиль микробиома у здоровых, бессимптомных пациентов и лиц с предрасположенностью к mesh-ассоциированным осложнения. С использованием такого таргетного фенотипирования возможно выявление групп пациентов с минимальным риском неблагоприятных исходов и максимальным преимуществом от имплантации сетчатых протезов.Литература
- Noé G.K. Genital Prolapse Surgery: What Options Do We Have in the Age of Mesh Issues? J. Clin. Med. 2021; 10: 267.
- Maher C., Yeung E., Haya N., Christmann-Schmid C., Mowat A., Chen Z., Baessler K. Surgery for women with apical vaginal prolapse. Cochrane Database of Systematic Reviews. 2023: 7.
- Glazener C., Breeman S., Elders A., Hemming C., Cooper K.G., Freeman R.M., Smith A. Mesh inlay, mesh kit or native tissue repair for women having repeat anterior or posterior prolapse surgery: randomised controlled trial (PROSPECT). BJOG 2020; 127: 1002–1013.
- Baessler K., Christmann-Schmid C., Maher C., Haya N., Crawford T.J., Brown J. Surgery for women with pelvic organ prolapse with or without stress urinary incontinence. Cochrane Database of Systematic Reviews. 2018; 8.
- Horosz E., Pomian A., Zwierzchowska A., Majkusiak W., Tomasik P., Barcz E. Does Previous Pelvic Organ Prolapse Surgery Influence the Effectiveness of the Sub-Urethral Sling Procedure? J Clin Med. 2020; 9 (3): 653.
- Digesu G.A., Bhide A.A., Swift S. Mid-urethral sling and the mystery of pain. Int Urogynecol J. 2022; 33(4): 749–50.
- Lundmark Drca A., Alexandridis V., Andrada Hamer M., Teleman P., Söderberg M.W., Ek M. Dyspareunia and pelvic pain: comparison of mid-urethral sling methods 10 years after insertion. Int Urogynecol J. 2024; 35(1): 43-50.
- Rovner E., de Tayrac R.,Kirschner‐Hermanns R., Veit‐Rubin N., Anding R. Is polypropylene mesh material fundamentally safe for use as a reconstructive material in vaginal surgery: ICI‐RS 2019? Neurourology and Urodynamics. 2020; 1–8.
- Hermieu N., Ouzaid I., Aoun R., Xylinas E., Hermieu J.F., Schoentgen N. Urethral Exposure of Mid-urethral Sling: Diagnosis, Management and Functional Outcomes. Urology. 2022; 164:100-105.
- Ерема В.В., Буянова С.Н., Мгелиашвили М.В., Ерема В.В., Петракова С.А. Mesh-ассоциированные осложнения при коррекции пролапса тазовых органов и стрессовой формы недержания мочи. Российский вестник акушера-гинеколога. 2021; 21(3): 74‑78.
- Deffieux X., Letouzey V., Savary D., Sentilhes L., Agostini A., Mares P., et al. Prevention of complications related to the use of prosthetic meshes in prolapse surgery: guidelines for clinical practice. Eur J Obstet Gynecol Reprod Biol. 2012; 165: 170–80.
- Daly J.O., Frazer M., Cartwright R., Veit-Rubin N., Giles M. The role of microbial colonisation and infection in pelvic floor mesh complications and implications for management: a commentary. BJOG. 2020; 127: 260–263.
- Fettweis J.M., Serrano M.G., Girerd P.H., Jefferson K.K., Buck G.A. A new era of the vaginal microbiome: advances using next‐generation sequencing. Chem Biodivers. 2012; 9(5): 965‐976.
- Veit-Rubin N., De Tayrac R., Cartwright R., Franklin-Revill L., Warembourg S., Dunyach-Remy C., Lavigne J.P., Khullar V. Abnormal vaginal microbiome associated with vaginal mesh complications. Neurourol Urodyn. 2019;38 (8): 2255-2263.
- Hawn M.T., Richman J.S., Vick C.C., Deierhoi R.J., Graham L.A., Henderson W.G. Timing of surgical antibiotic prophylaxis and the risk of surgical site infection. JAMA Surg. 2013; 148:7: 649-657.
- Попов А.А., Идашкин А.Д., Тюрина С.С., Будыкина Т.С. Возможности использования программы ускоренного восстановления в коррекции течения послеоперационного периода при хирургическом лечении в гинекологии. Российский вестник акушера-гинеколога. 2019; 19(6): 23-30.
- Попов А.А., Федоров А.А., Идашкин А.Д. Реализация программы ускоренного восстановления у пациенток, оперированных лапароскопическим и робот-ассистированным доступом в гинекологии. Информационно-методическое письмо. 2021; 24.
- Шуршалина А.В., Кречетова Л.В., Зиганшина М.М., Сухих Г.Т. Локальное действие эпиген интим спрей (глицирризиновая кислота) при вирусных инфекциях половых органов. Акушерство и гинекология. 2009; 3: 63-5.
- Рахматулина М.Р., Большенко Н.В. Опыт применения активированной глицирризиновой кислоты при вульвовагинитах, цервицитах и генитальной папилломавирусной инфекции. Акушерство и гинекология. 2019; 9: 153-158.

